A che punto sono gli studi clinici con i famaci Mavacamten e Aficamten?

Prof. Iacopo Olivotto
Gli studi clinici con Mavacamten sono completati per quanto riguarda la registrazione del farmaco per le cardiomiopatie di tipo ostruttivo. In molti paesi per i pazienti con ostruzione il farmaco è già disponibile e rimborsabile, in Italia probabilmente sarà ancora necessario un anno per avere la rimborsabilità. Nel frattempo possiamo procedere con l’uso compassionevole per i pazienti con indicazioni precise. Invece, per le forme non ostruttive è in corso uno studio che si chiama Odissey che finirà tra un paio d’anni. Abbiamo finito adesso l’arruolamento dei pazienti, e appena l’ultimo paziente avrà finito il trattamento dovremo attendere un paio d’anni per vedere i risultati ottenuti. Per quanto riguarda Aficamten lo studio sulle forme ostruttive è finito e verrà presentato in primavera, per il non ostruttivo lo studio è in corso e deve essere ancora completato l’arruolamento.
Possiamo spiegare cosa si intende per uso compassionevole? Quanti pazienti sono o saranno coinvolti?
L’uso compassionevole non è più sperimentazione, significa che il farmaco è già disponibile e si chiede alla ditta produttrice di fornirlo ai pazienti con indicazione in attesa che il farmaco diventi rimborsabile.
Al momento non ci sono pazienti in Italia perché questa fase è partita a gennaio, noi stiamo inviando alla Ditta produttrice le schede con i dati anonimizzati dei pazienti che reputiamo idonei. Il produttore deve dare la sua approvazione. A quel punto ci verrà inviato il farmaco per ognuno dei vari pazienti. È un impegno grosso, richiede molti controlli e molta burocrazia. Ci attendiamo a livello italiano oltre un centinaio di pazienti, ma in Italia non c’è un tetto all’ingresso di pazienti per l’uso compassionevole. È importante in questa fase che il farmaco sia utilizzato da mani esperte perché un farmaco nuovo se dato al paziente sbagliato potrebbe creare problemi, sarebbe un peccato rischiare così di rovinare la reputazione a un farmaco che invece ha una grande potenzialità.
Ci sarà un registro italiano che collezionerà i dati dei pazienti e che sarà coordinato dall’Università di Firenze e un board che comprende una decina di centri italiani dove lavorano gli esperti della patologia. Ci sono già una ventina di centri che hanno chiesto di partecipare, e forse si potrebbe arrivare a una quarantina.
Qual è la differenza di azione dei due farmaci? In futuro ce ne saranno altri nuovi?
La differenza più importante è che Mavacamten ha un’emivita molto lunga, circa nove giorni. Questo vuol dire che per avere un effetto pieno bisogna aspettare almeno un mese e quindi ha anche una titolazione anche lenta, il processo per arrivare alla dose ottimale per il paziente può durare anche sei mesi. Inoltre può avere alcune interazioni con alcuni farmaci come farmaci antifungini e antiretrovirali.
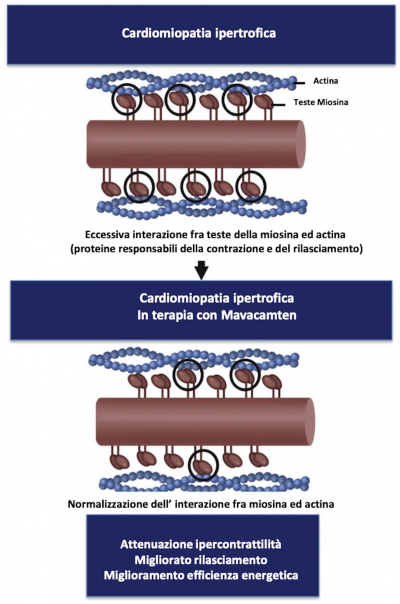 L’Aficamten è più rapido, la titolazione si può fare in meno di due mesi e non dovrebbe avere le stesse interazioni. Il fatto che ha vita più breve può essere visto in due modi: da una parte si fa prima la titolazione, dall’altra con un paziente che risponde in maniera anomala è più rapido l’instaurarsi di un problema. Con il Mavacamten avviene tutto più lentamente ma è più lento anche il “washout”, cioè la fine dell’effetto. Possiamo concludere dicendo che il profilo è molto simile sia come sicurezza che come efficacia. I pazienti hanno una risposta molto paragonabile, la scelta su quale farmaco utilizzare dipenderà principalmente dalle interazioni con gli altri farmaci e dai costi.
L’Aficamten è più rapido, la titolazione si può fare in meno di due mesi e non dovrebbe avere le stesse interazioni. Il fatto che ha vita più breve può essere visto in due modi: da una parte si fa prima la titolazione, dall’altra con un paziente che risponde in maniera anomala è più rapido l’instaurarsi di un problema. Con il Mavacamten avviene tutto più lentamente ma è più lento anche il “washout”, cioè la fine dell’effetto. Possiamo concludere dicendo che il profilo è molto simile sia come sicurezza che come efficacia. I pazienti hanno una risposta molto paragonabile, la scelta su quale farmaco utilizzare dipenderà principalmente dalle interazioni con gli altri farmaci e dai costi.
Poi ci sono altre molecole in via di sperimentazione: una simile all’Aficamten ovvero un Mavacamten più rapido. Altre aziende americane stanno mettendo a punto altre piccole molecole, come piccoli proiettili di precisione, con azione simile al Mavacamten ma che agiscono su fasi diverse del ciclo cardiaco.
Non solo, ci sono farmaci con azione diversa, che agiscono migliorando l’azione dei mitocondri, che nelle cellule controllano la produzione di energia. Sono farmaci che sono stati sviluppati più per le cardiopatie del diabetico ma pare che funzionino anche per le cardiomiopatie in particolare per le forme ipertrofiche. Sono meno rivoluzionari ma molto interessanti.
Inoltre, per la prima volta è stata somministrata una terapia genica a un paziente con Cardiomiopatia ipertrofica, un progetto davvero ambizioso il cui risultato ancora è molto difficile da prevedere.
Cosa significa per i pazienti affetti da cardiomiopatie la possibilità di essere trattati con questi farmaci? Quanto può migliorare grazie all’uso di questi farmaci la qualità della vita di questi pazienti?
Se i pazienti hanno forme ostruttive la qualità della vita cambia in maniera radicale, alcuni si rendono conto per la prima volta nella vita cosa vuol dire star bene. Altri hanno sintomi più recenti quindi tornano a come stavano tanti anni prima. Il risultato è paragonabile a quelli ottenuti con la chirurgia (“miectomia”). In alcuni pazienti i risultati sono stati stupefacenti, è davvero qualcosa che cambia la qualità della vita.
Il problema è sempre quello della sicurezza, perché possono succedere degli eventi che creano degli allarmi. Tuttavia dopo 5 anni di esperienza, è improbabile che si abbiano, ma è presto per poter cantare vittoria. L’azienda può sempre bloccare la produzione in caso di eventi avversi gravi.
Un aspetto problematico è costituito dal prezzo. Negli Stati Uniti questi farmaci sono partiti con un prezzo di 80/90 mila euro l’anno, da noi si arriverà forse ad un terzo di questa cifra, cioè intorno ai 20/30 mila euro, perché nella prima fase le aziende farmaceutiche devono recuperare i costi degli studi che sono molto alti. Ma dopo questa fase è possibile che i prezzi calino ancora molto perché questi farmaci non sono costosi da sintetizzare e la materia prima costa poco. Se usciranno diversi di questi farmaci, ci sarà competizione e se ci saranno tanti pazienti, è prevedibile che questo accada. Se lo stesso farmaco fosse stato sviluppato per lo scompenso cardiaco e non per la cardiomiopatia ipertrofica lo stesso farmaco oggi costerebbe meno di cento euro al mese. Sicuramente se le indicazioni saranno confermate questo farmaco potrebbe diventare un farmaco standard per i pazienti con Cardiomiopatia ipertrofica. A quel punto con milioni di pazienti che potrebbero usarlo, il prezzo potrebbe avvicinarsi a quello dei comuni farmaci dello scompenso.
C’è altro da aggiungere per dare ai pazienti un’informazione corretta riguardo a questi farmaci?
Dare un’informazione corretta è molto importante. La prima cosa da capire è che ricevere la diagnosi di cardiomiopatia non vuol dire automaticamente aver accesso al farmaco perché il farmaco ha delle indicazioni molto precise per i pazienti che hanno le stesse caratteristiche dei pazienti dello studio clinico, cioè pazienti con CMI ostruttiva. E’ importante non creare false aspettative. Il secondo punto è che l’accesso al farmaco consta di un protocollo molto complesso e di un’importante organizzazione che non tutte le strutture sono in grado di garantire, soprattutto in questo momento in cui le strutture sanitarie sono oberate di lavoro e richieste. Ma quanto abbiamo visto finora con le sperimentazioni ci dà grandi speranze.